:::
- 首頁
- /
- 年度
- /
- 2021
- /
- 精準健康(生技&新藥)
- /
- 一種TMD1蛋白質用於製備發炎性骨流失藥物的用途
| 技術名稱 | 一種TMD1蛋白質用於製備發炎性骨流失藥物的用途 | ||
|---|---|---|---|
| 計畫單位 | 高雄醫學大學 | ||
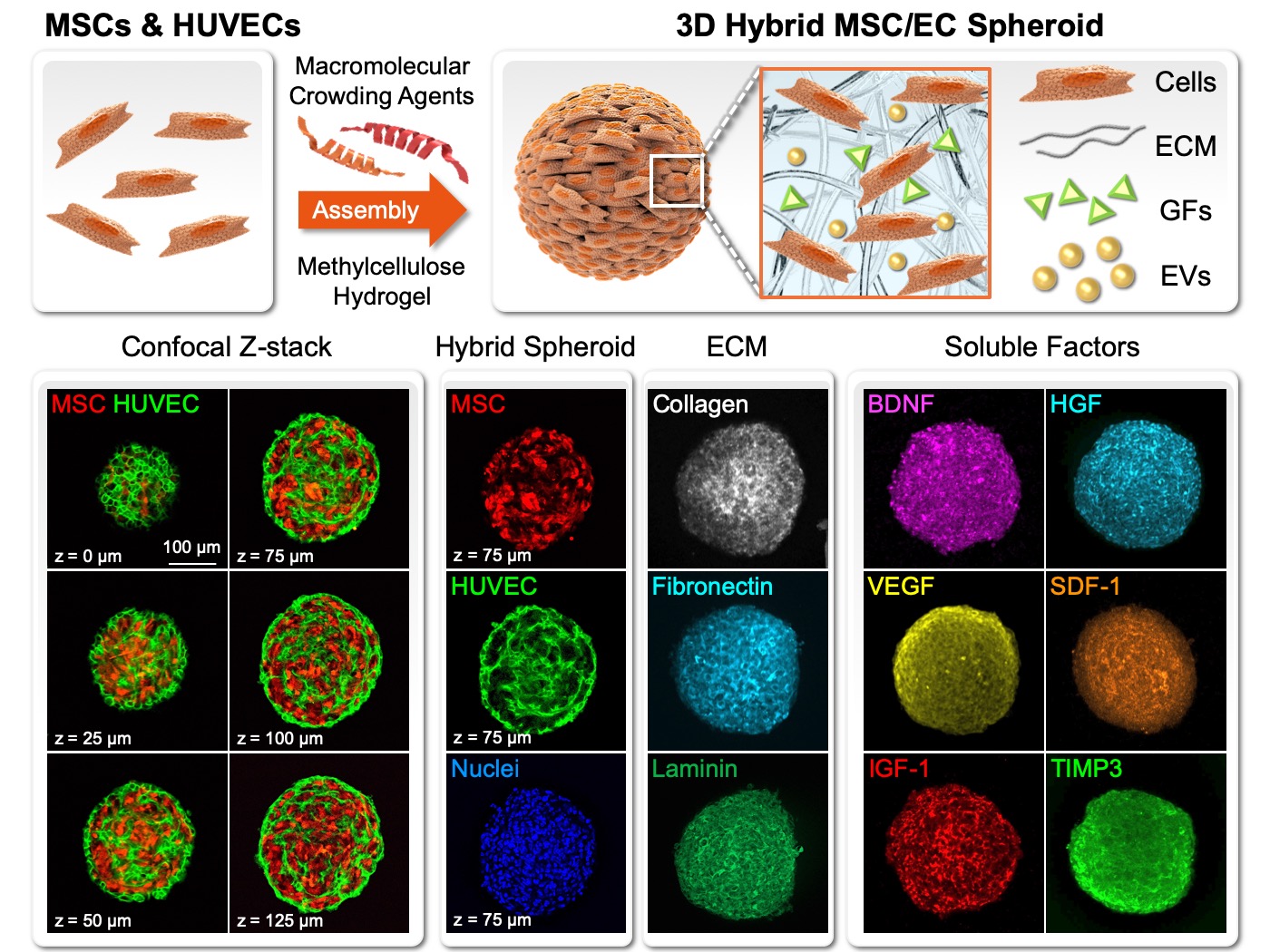
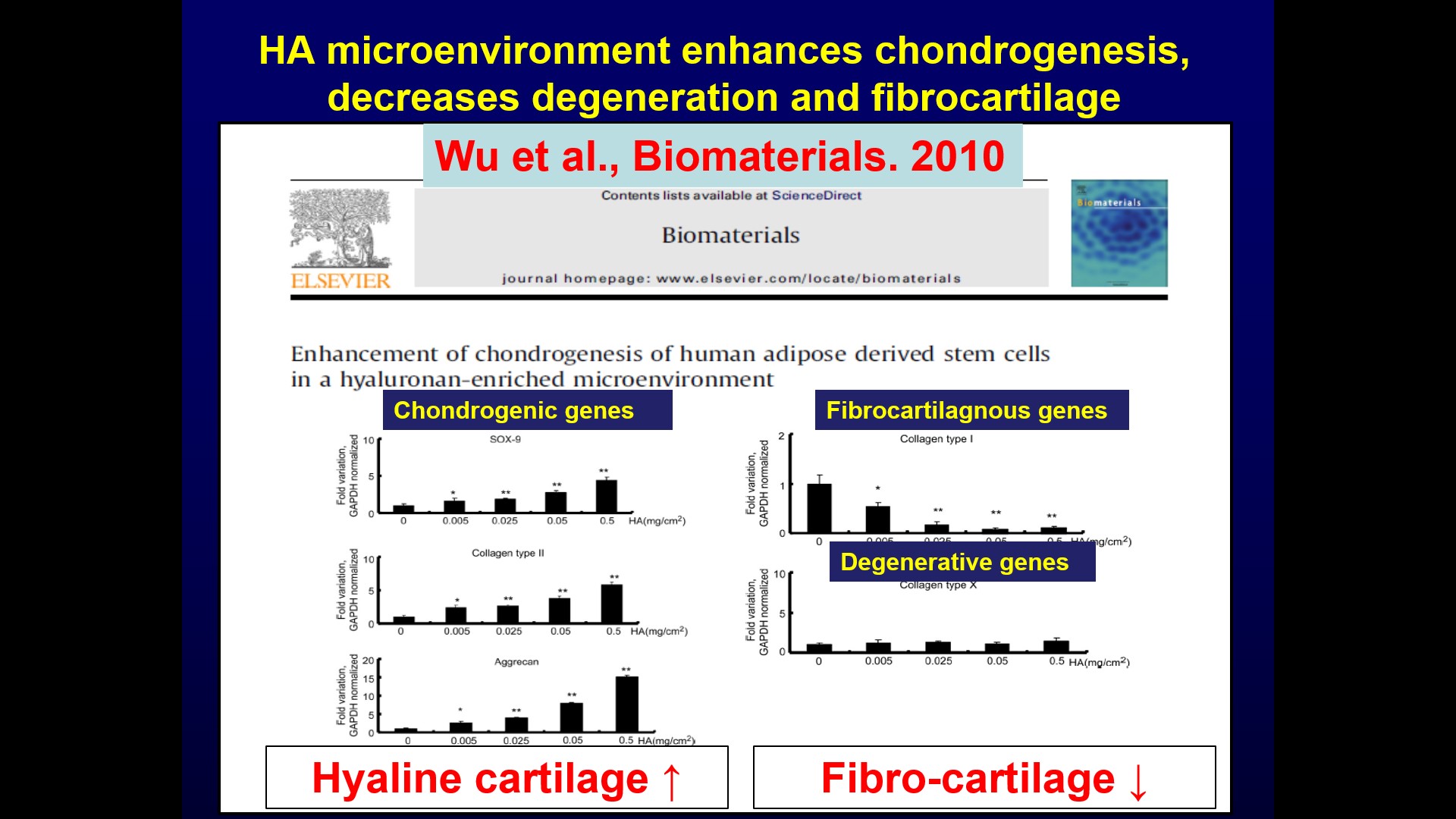
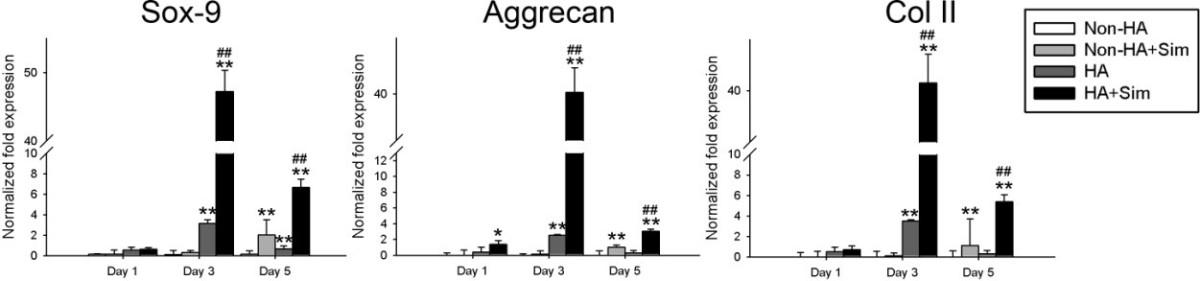
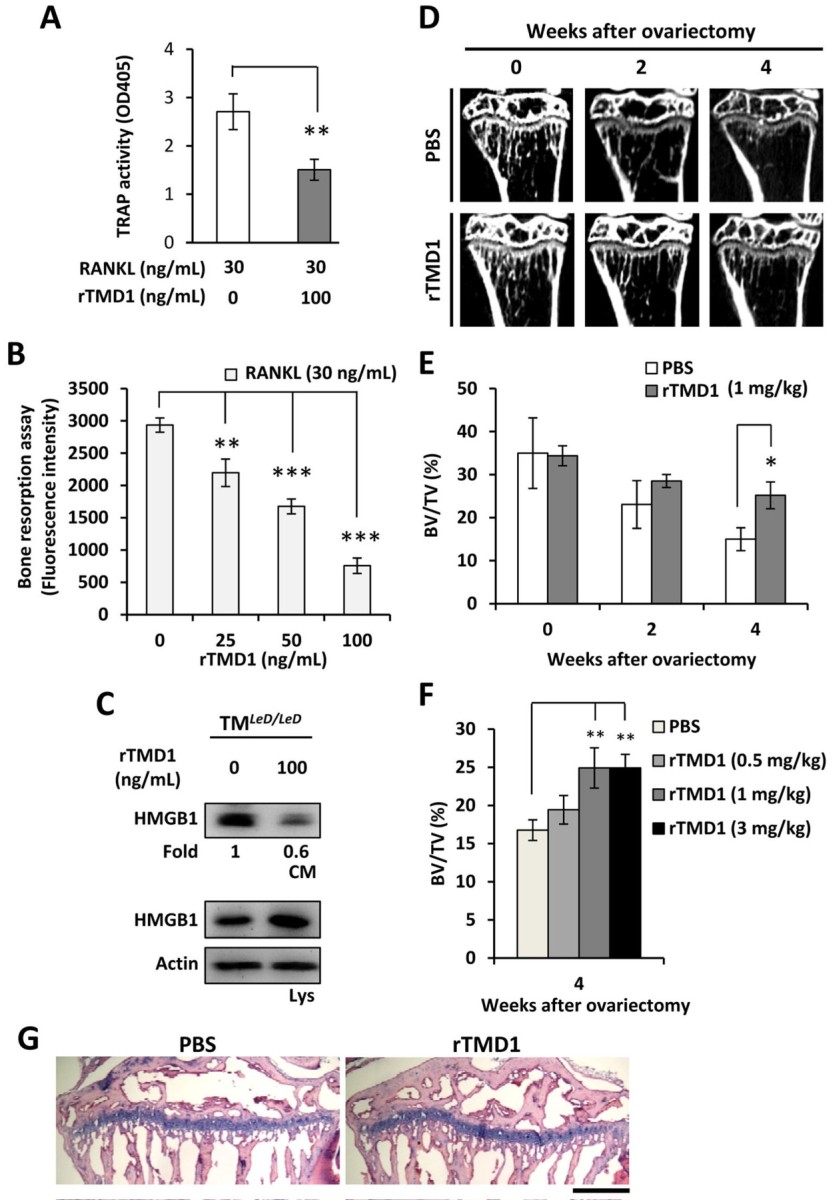
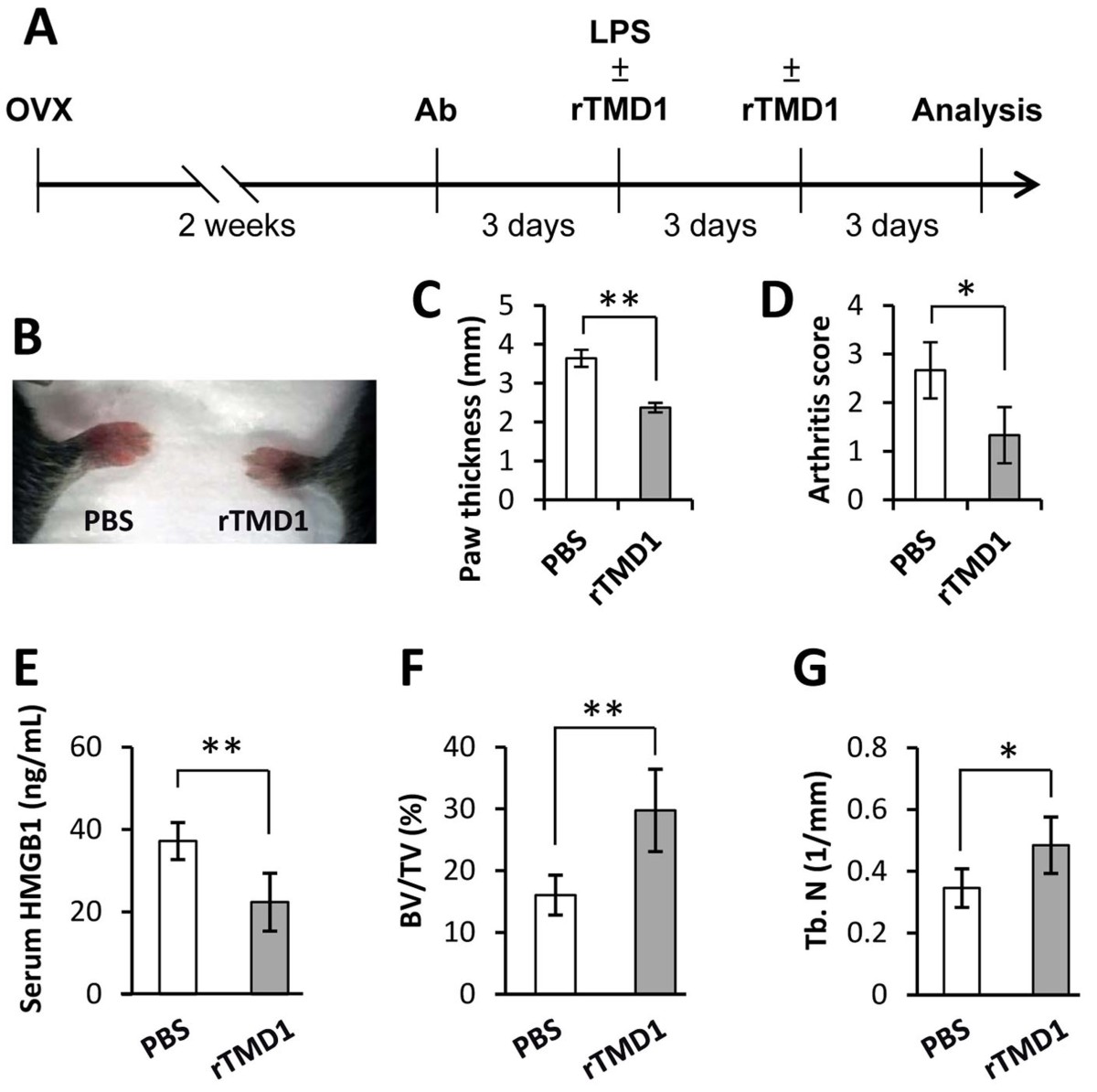
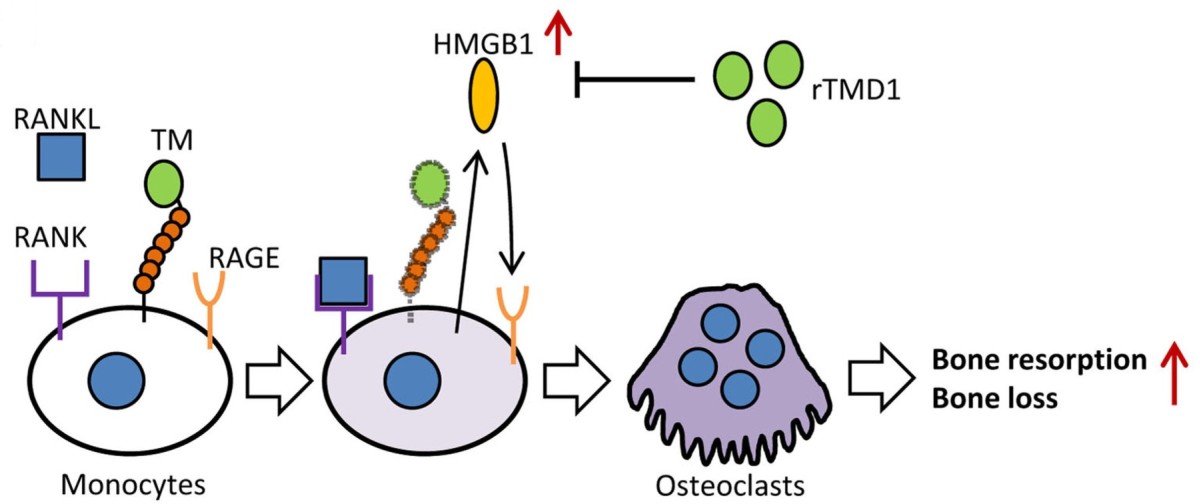
| 技術簡介 | 越來越多的研究結果顯示,過多的發炎反應會促進體內蝕骨細胞(osteoclasts)的形成,進而導致骨質流失或骨密度下降,最終造成一系列的相關疾病,例如:骨質疏鬆症(osteoporosis)、骨疼痛(bone pain)、類風濕性關節炎(rheumatoid arthritis)…等。細胞核kB受體活化因子配體(RANKL)是誘導骨髓前驅細胞分化形成蝕骨細胞與骨溶蝕活性的重要因子。RANKL的作用機制是促使骨髓前驅細胞分泌高遷移率族蛋白B1 (HMGB1)到細胞膜外,再藉由HMGB1與前驅細胞膜上的高糖化終產物接收器(RAGE)結合進而完成蝕骨細胞的形成與活化。另一方面,文獻指出,凝血酶調節素的類凝集素功能區(thrombomodulin lectin-like domain, TMD1)具有干擾HMGB1-RAGE交互作用,而達到抑制發炎的效果。然而,凝血酶調節素在骨代谢中的生理功能和可能的應用卻不清楚。因此,本團隊利用RANKL誘發RAW264.7巨噬細胞形成類骨細胞的模式和組織特異性基因操縱技術我們首先證明了TMD1是蝕骨細胞生成作用的負向調節者,而在巨噬細胞中缺失TMD1則會增強的蝕骨細胞的形成。進一步,給予TMD1能夠顯著減少卵巢切除誘發骨質疏鬆動物模式與類風濕性關節炎小鼠動物模型的骨質流失。因此,我們認為TMD1應該是一種可用於治療骨質流失相關疾病的新穎蛋白質藥物。 |
||
| 科學突破性 | 本案的目的是在於治療骨質流失之疾病,因目前人們會因生理因素或其他外在因素而有骨質的流失或骨密度的下降的問題,會導致骨質疏鬆症,其會有骨折、腰酸背痛、行動能力受限,甚至無法行動等現象發生。一般來說,人體的骨骼會不斷更新,以維持強韌而優良的品質,而年輕時「造骨」速度高於「蝕骨」速度,因此骨質總量及骨質密度得以持續上昇;而到35歲左右,骨質密度達到顛峰,稱之為「尖峰骨本」。但伴隨年齡增長,骨質流失的速度要高於骨質製造的速度,於是骨質密度逐漸下降。其中,蝕骨細胞是造成骨質流失的主因之一,而本案正是透過抑制Receptor activator of nuclear factor-κB ligand (RANKL)所誘導的蝕骨細胞生成,以達到治療骨質疏鬆症之效果。 |
||
| 產業應用性 | 全球老年人口逐漸增加,因此骨質流失相關病變的預防與治療將是一個相當無法忽視的課題。 |
||
其他人也看了