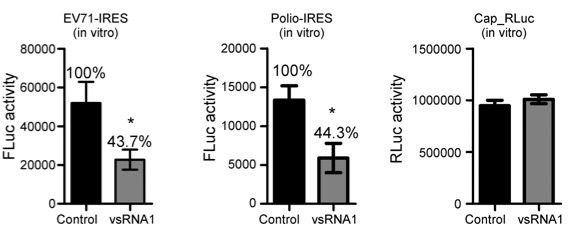
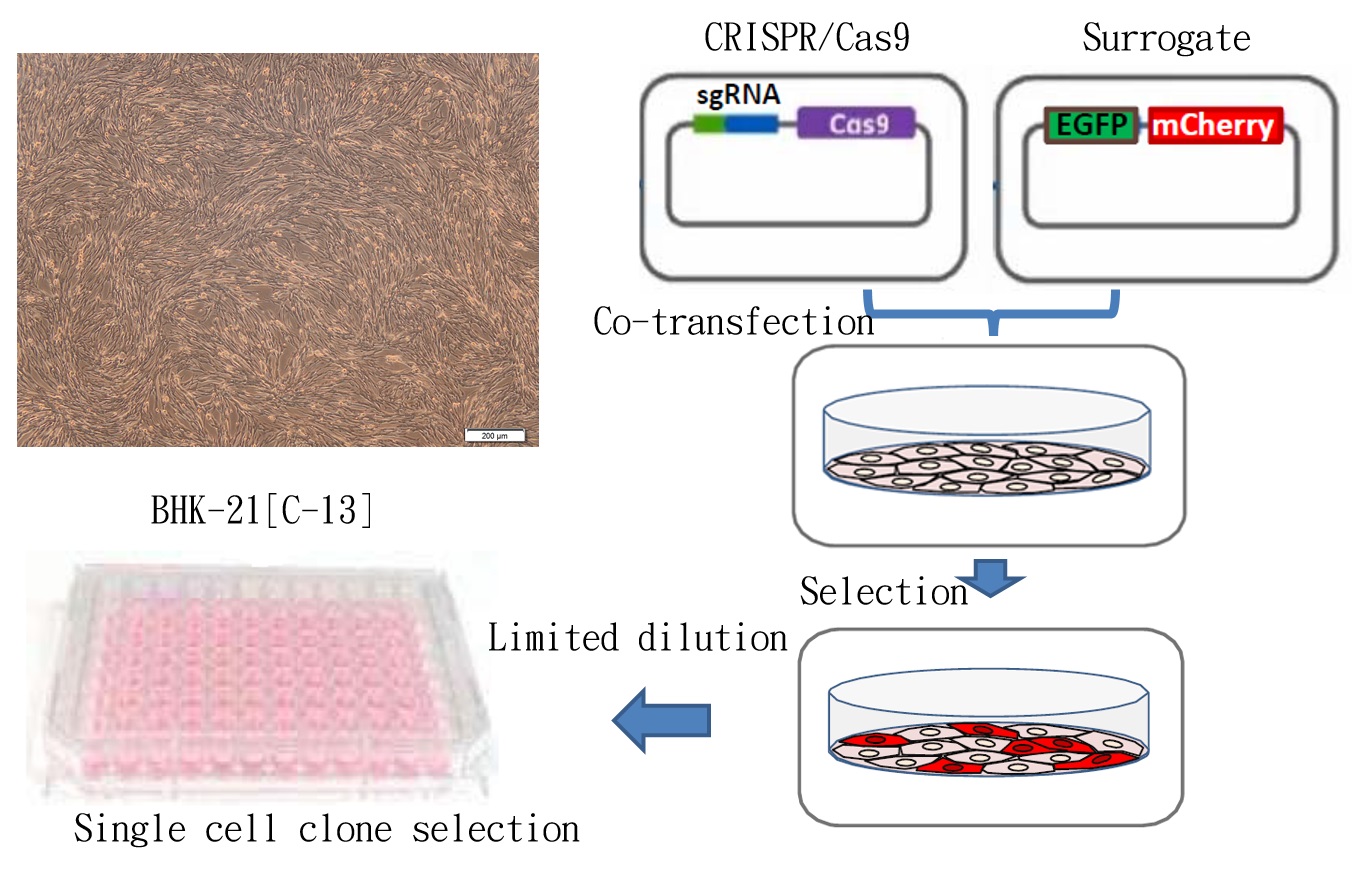
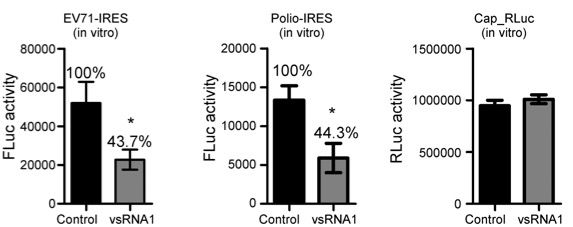
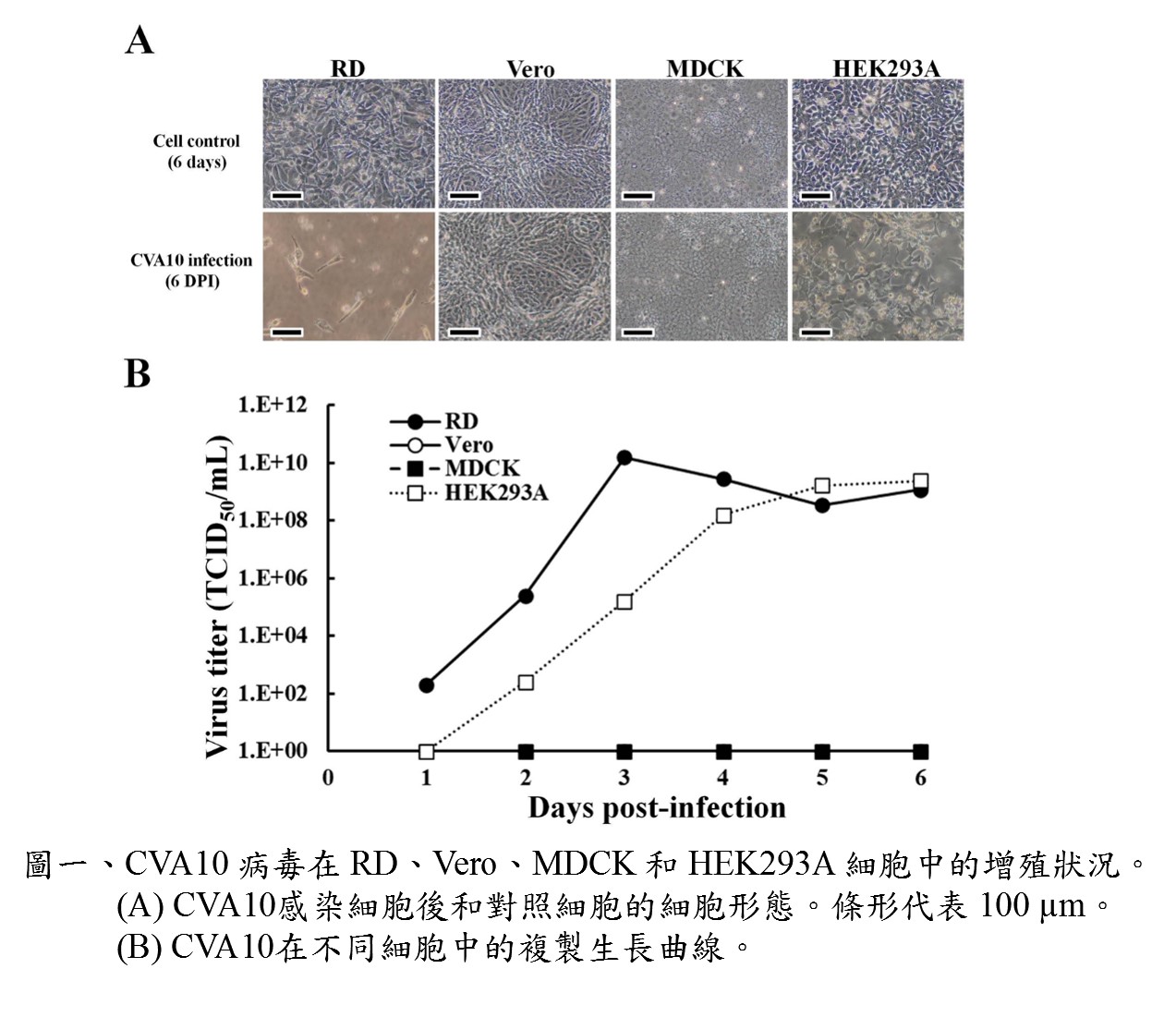
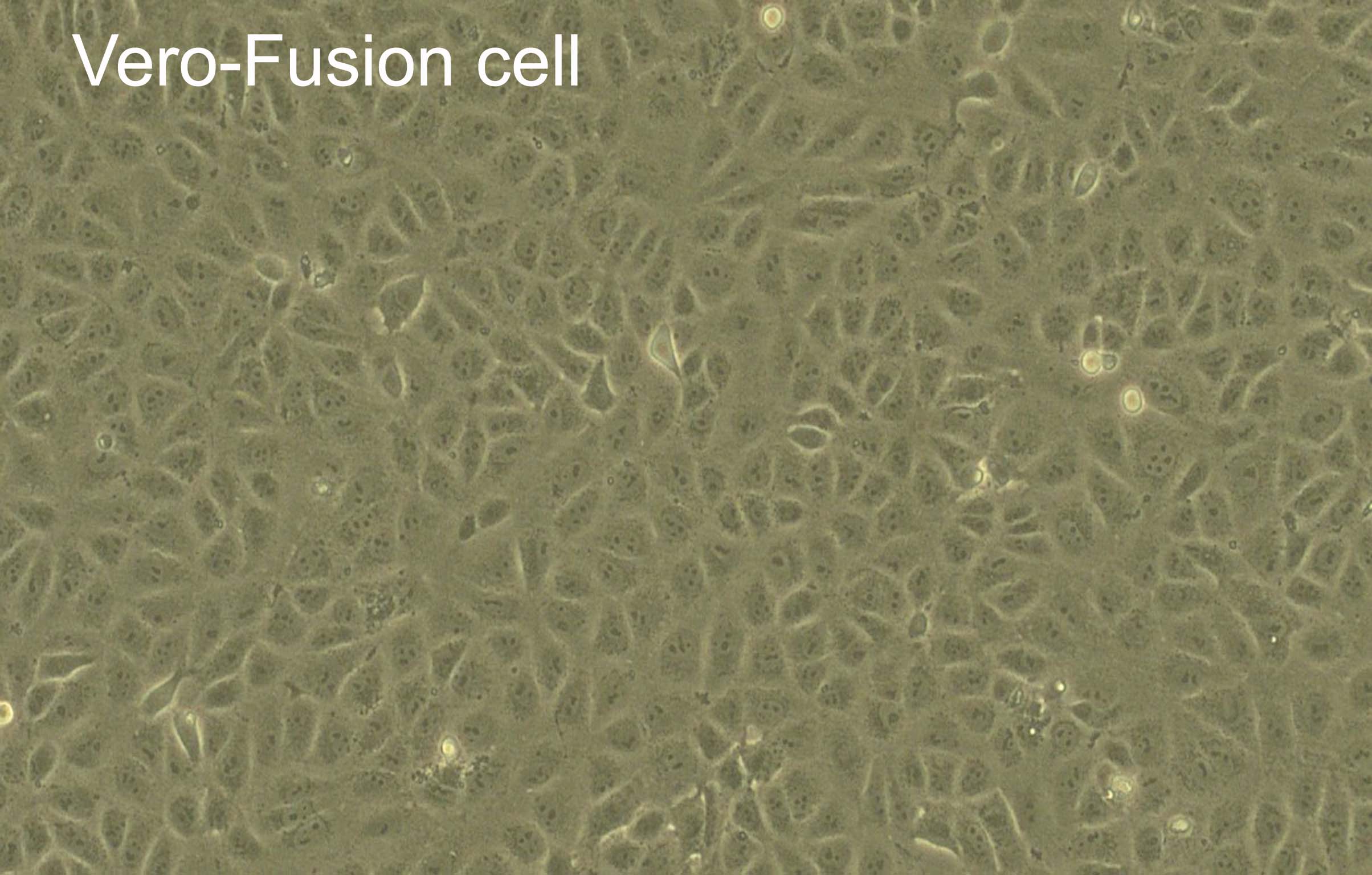
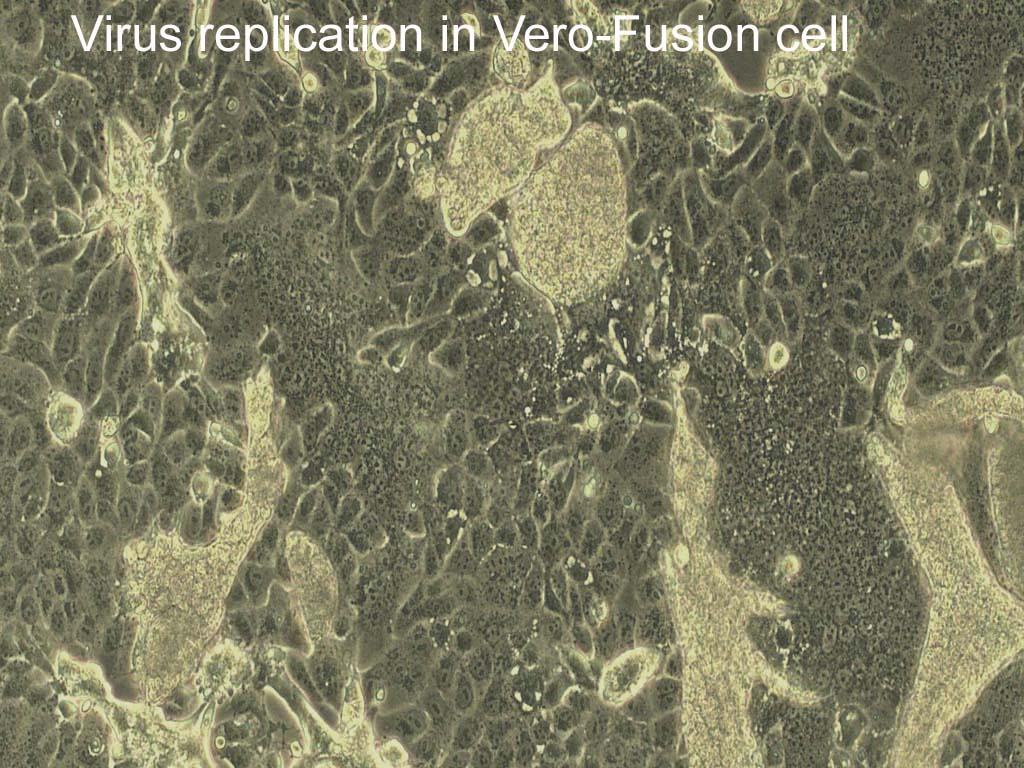
"病毒疫苗細胞生產技術平台”之技術包含: 1.細胞及病毒之選殖技術 (製備適應病毒生產之細胞株)。2.細胞表現病毒接受體技術 (使病毒快速接種細胞)。3.阻斷細胞抗病毒機制(縮短病毒大量複製時間)。 4.初代細胞永生化技術(達成工業化穩定產能之目的)。5.細胞無血清全懸浮培養技術(去除血清培養汙染疫苗之可能性)。有效穩定病毒在細胞高增殖量取決於技術上克服細胞對於病毒接種後免疫反應與細胞凋亡造成病毒複製中止。以基因工程技術克服病毒接種後免疫反應與細胞凋亡,讓宿主細胞表現細胞表面專一性病毒受體蛋白,有效降低病毒接種後免疫反應與細胞凋亡,提供病毒快速繁殖之細胞內環境,強化宿主細胞對病毒之易感性,並篩選培育出適應多種病毒接種之細胞株vero、BHK21、MDCK、RD、COS1、COS7、HeLa、MAC145、MA104…等,並有效增殖疫苗開發所需病毒,例如人類流感病毒、腸病毒、腺病毒、泡疹病毒、副流感病毒、呼吸道融合病毒或動物Influenza virus、Newcastle disease virus、PRRS virus、Avian reovirus、Infectious bursal disease virus、PED virus等。能以傳統懸浮細胞培養系統進行病毒生產,製程過程不需額外進行處理或添加生態或化學藥劑調控細胞生長周期,使製程單純化並降低成本。研究數據顯示能在相同時間內比其他細胞病毒生產方式,增加1000倍產量。本製程以細胞培養病毒,無需加入動物血清,可去除疫苗生產過程可能汙染來源, 本技術已成功運用於第VII基因型新城病不活化疫苗、細胞培養傳染性華氏囊炎疫苗,家禽營養不良症候群疫苗、雞腎臟型傳染性支氣管炎疫苗、細胞培養新城病活毒疫苗、豬流行性下痢病毒疫苗、假性狂犬病疫苗之開發,顯著減少抗原生產成本。以細胞培養取代動物犧牲之相關科技生產技術是世界趨勢,本技術能替代傳統以動物製備疫苗所需之病毒的生產方式,有利於技術推廣至歐美等先進國家。 |