| 技術名稱 | 新穎奈米載體-脂蛋白顆粒遞送CRISPR/Cas9基因修復元件作為眼科遺傳疾病基因修正之平台 | ||
|---|---|---|---|
| 計畫單位 | 國立陽明大學 | ||
| 計畫主持人 | 邱士華 | ||
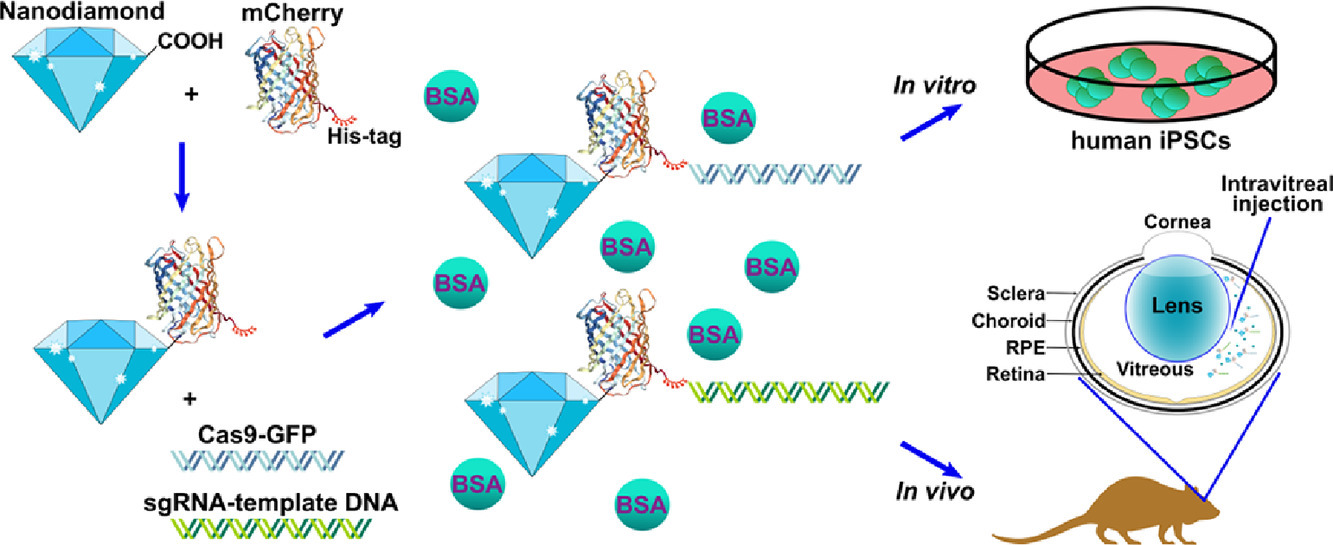
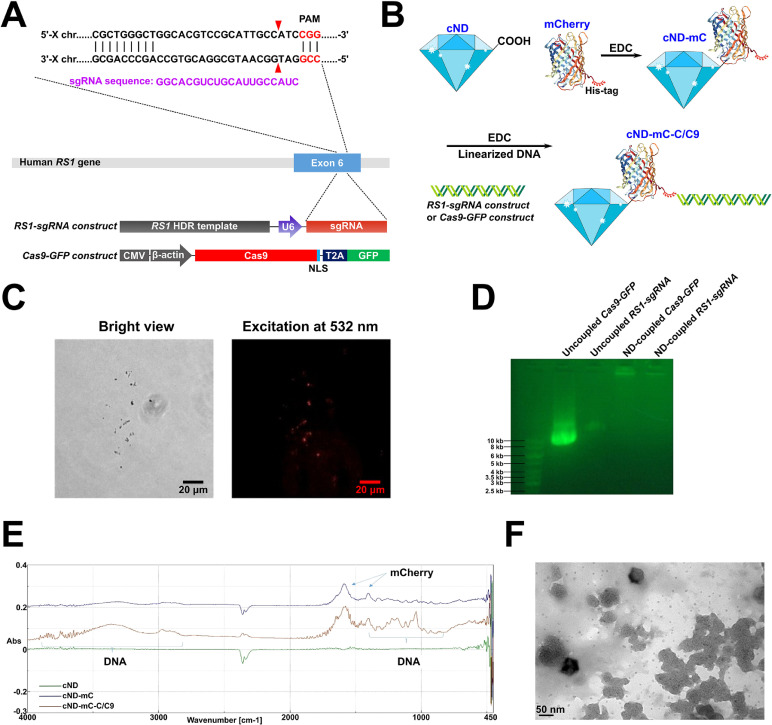
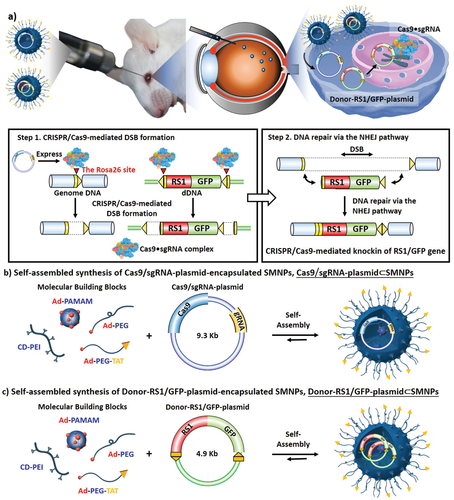
| 技術簡介 | X染色體性連鎖視網膜分裂症是因為RS1基因缺陷,導致早發先天性黃斑部病變和嚴重視力喪失。然而,如何使用安全的基因組編輯技術來有效、精確地修復XLRS的基因仍然模糊不清。CRISPR/Cas9是一種高效,精確且經濟高效的基因組編輯技術,為多種人類疾病提供潛在的治療方案。基於CRISPR的技術,開發了利用NHEJ途徑的同源性獨立靶向整合(HITI)技術且能高效率地進行活體基因敲入。當前CRISPR技術主要採用病毒載體運輸,然而,病毒載體受限於乘載空間不足和安全性的考量,因此,非病毒傳遞方法有其必要性。本計畫將探索基於CRISPR的HITI基因編輯材料包裹到超分子納米顆粒(SMNP),然後通過SMNP傳遞方法,將其傳遞到特定細胞及XLRS病患誘導多能幹細胞衍生3D視網膜類器官和小鼠視網膜中進行基因敲入,達到表達RS1的可能性。因此,本研究的目標如下:1)採用小規模組合篩選獲得Cas9/sgRNA-質體ÌSMNPs和Donor DNAÌSMNPs最佳遞送效率的配方,2)測試是否可利用自我組裝的奈米載體將Cas9 / sgRNA質體和Donor-RS1/GFP質體共同遞送到細胞中來實現RS1基因敲入,3)探索使用SMNPs策略在老鼠眼睛進行RS1基因敲入,建立基因替代療法,4)通過SMNPs技術將基因敲入XLRS-hiPSCs衍生的3D視網膜類器官。本計畫將有助於開發新型基因治療技術,特別是患有遺傳性眼睛疾病的患者提供新一代的治療方法。 |
||
| 科學突破性 | 奈米鑽石可以被iPSC和小鼠視網膜內化,引入RS1基因特異性突變修正。奈米鑽石與BSA的混合顯著增加了細胞的攝取。我們證明了CRISPR-Cas9攜載之奈米鑽石可治療小鼠視網膜的感光細胞缺陷,這是XLRS典型病徵。因此,我們建立的奈米鑽石基因修正平台在治療XLRS體內和體外疾病模型方面具有巨大潛力。 |
||
| 產業應用性 | 我們開發的基因治療技術是有效的、具有高度的生物安全性,可以大量標準化生產。 非病毒性的基因治療載體有其必要性,符合臨床需求的趨勢,帶來基因療法上突破性的影響。進一步將開發用於遺傳性疾病的有效治療藥物,人類誘導型多能幹細胞(iPSC)將用作各種疾病的測試平台。此外,將展開合作以增強基因編輯療法的技術。 |
||
| 關鍵字 | 奈米鑽石 奈米顆粒 X染色體串聯視網膜裂損症 人類誘導型多能幹細胞 基因編輯 遺傳性視網膜疾病 小鼠視網膜 | ||
- 聯絡人
- 林益瑩
- 電子信箱
- s19609005@gm.ym.edu.tw
其他人也看了